CONTEXTUALIZAÇÃO
“[…] A grande variedade de patógenos e métodos de teste disponíveis torna os testes microbiológicos desafiadores e, portanto, a detecção e a correção de erros são componentes importantes dos testes de laboratório de microbiologia de qualidade […]. Os microbiologistas clínicos devem ser especialistas em todos os aspectos das fases pré-analítica, analítica e pós-analítica dos testes microbiológicos. Devemos educar os clínicos sobre os aspectos críticos da seleção de testes, coleta e transporte de amostras e interpretação de resultados que ocorrem fora do laboratório”.
Fonte: Science Direct. Enciclopédia de Microbiologia: Microbiologia Clínica, 4ª ed., 2019. Disponível em: https://www.sciencedirect.com/topics/immunology-and-microbiology/clinicl-microbiology. Acesso em: 03/06/2025.
A integração do conhecimento teórico com a prática é fundamental para capacitação do profissional, trazendo agilidade e assertividade nos resultados. Esta atividade traz, através de um estudo de caso, questões que visam alinhar os conhecimentos teóricos com os práticos através de problemáticas que são frequentes na rotina do microbiologista clínico.
ESTUDO DE CASO
Imagine que você é um microbiologista em um laboratório de análises clínicas de um hospital e, na sua rotina de trabalho, recebe diariamente diversas amostras biológicas. Essas amostras são provenientes tanto dos setores de internação, quanto de atendimentos ambulatoriais ou de emergência.
Sua função é executar os procedimentos técnicos, avaliar os controles de qualidade e treinar os funcionários que trabalham no setor.
Iniciando sua rotina de trabalho, enquanto avaliava o controle de qualidade semanal, você identificou alguns problemas que interferem diretamente no andamento das análises, mas que com ajustes básicos e orientações ou treinamentos da equipe técnica, podem ser resolvidos. Diante disso, para capacitar e atualizar os técnicos do setor, você elaborou um guia teórico com as orientações necessárias.
ETAPA 1: Análise de erros pré-analíticos
Você identificou problemas na coleta e semeadura de amostras. Isso impacta negativamente no isolamento de colônias, atrasando a identificação dos microrganismos e no tratamento dos pacientes.
Questão 1:
A escolha do tipo de semeadura é essencial para garantir o isolamento, a interpretação das culturas e execução dos testes. Essas técnicas podem ser dividias em semeaduras qualitativas, utilizadas quando se busca detectar a presença de patógenos, independentemente da quantidade; e quantitativas, usadas quando é importante saber a quantidade de bactérias por volume de amostra. Desta forma, RESPONDA:
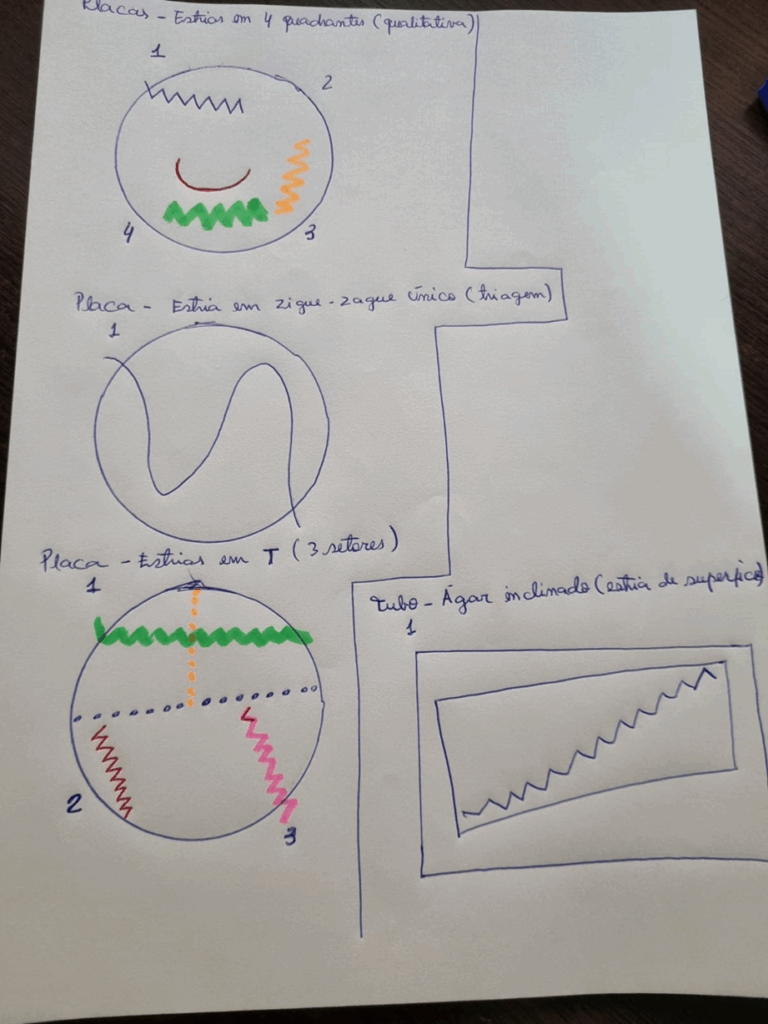
a. DESCREVA e ILUSTRE manualmente as técnicas de semeadura qualitativa por estrias em meios sólidos, tanto em tubos, quanto em placas:
Na placa em 4 quadrantes, esterilize e resfrie a alça; faça zigue-zague no 1º setor. Flambe/resfrie, puxe 2–3 vezes do setor anterior e estrie o 2º; repita para 3º e 4º, com traços finos para diluir o inóculo.
Na placa em T (3 setores), estrie o setor superior; flambe/resfrie, puxe 2–3 vezes para o setor inferior esquerdo e estrie; repita do inferior esquerdo para o inferior direito.
Na placa em zigue-zague único, faça um único serpenteado amplo pela superfície (uso de triagem/presença, sem foco em isolamento).
Em tubo com ágar inclinado (slant), mantenha o tubo inclinado e faça um zigue-zague superficial único da base ao topo, sem perfurar o meio.
Assim, as regras gerais: flambar e resfriar a alça entre setores, evitar encostar nas bordas/condensação, não “carregar” muito inóculo na primeira passada e incubar placas invertidas..
b. A contagem de colônias é essencial para a classificação entre infecção e contaminação. A técnica de semeadura quantitativa é aplicada também a outros tipos de materiais clínicos. CITE, ao menos três amostras que devem ser semeadas desta forma e DESCREVA como o procedimento é feito, da semeadura até a contagem das colônias.
Urina, lavado broncoalveolar/aspirado traqueal e ponta de cateter são amostras que a gente semeia de forma quantitativa para saber se há infecção de verdade ou só contaminação. Na urina, primeiro misturo bem, pego uma alça calibrada (de 1 µL ou 10 µL), faço um traço e espalho em zigue-zague na placa; depois de incubar, conto as colônias e transformo em UFC/mL: se usei 1 µL, multiplico por 1.000; se usei 10 µL, por 100. No lavado broncoalveolar/aspirado traqueal, homogeneizo (se estiver grosso, uso um mucolítico), faço diluições simples, planto um volume conhecido na placa e, após incubar, escolho a placa que tem uma quantidade “boa” de colônias (nem pouca, nem demais) para contar e calcular as UFC por mL. Já na ponta de cateter, corto um pedaço e apenas rolo a ponta quatro vezes sobre o ágar; depois de incubar, conto o número de colônias que cresceram nessa trilha e informo como UFC por ponta, valores mais altos costumam indicar que o cateter está realmente colonizado.
Questão 2:
A coleta é um ponto crucial, que pode inviabilizar complemente a análise dos materiais, causando gastos desnecessários e retrabalho. Além disso, o paciente terá que voltar ao laboratório ou será submetido a novo procedimento invasivo para a recoleta. Nos seus relatórios de pedido de recoleta por amostras inadequadas, a hemocultura tem sido a mais frequente, evidenciando uma dificuldade nos técnicos durante a coleta. Sendo assim, ELABORE um Procedimento Operacional Padrão (POP) sobre a coleta de hemocultura, abordando os tópicos abaixo:
a. Número de amostras e intervalo de tempo entre as punções.
– Adultos (suspeita geral de bacteremia/sepsis): coletar 2 conjuntos (cada conjunto = 1 frasco aeróbio + 1 anaeróbio) antes do antibiótico, de locais distintos, com 15–30 min entre si (se possível). Em instabilidade, coletar os 2 conjuntos em sequência e iniciar antibiótico.
– Endocardite/hemocultura difícil: 3 conjuntos nas primeiras 1–2 h ou até 24 h.
– Pediatria: geralmente 1–2 conjuntos conforme peso/volume disponível.
b. Volume de sangue e locais de punção.
– Adultos: 20–30 mL por conjunto (ideal: 10 mL em cada frasco aeróbio e anaeróbio). O volume é o fator mais crítico para positividade.
– Pediatria: usar frasco pediátrico; coletar 1–3 mL (lactentes) ou conforme tabela de peso/idade; priorizar aeróbio quando o volume for baixo.
– Locais de punção: venopunção periférica (preferencial) em dois sítios diferentes; evitar coleta por cateter/port (usar apenas se sem acesso periférico ou para investigação de infecção relacionada a cateter).
c. Procedimento de coleta.
- Identificar paciente e higienizar mãos; paramentar EPI.
- Antissepsia das tampas dos frascos (álcool 70%) e da pele: clorexidina alcoólica 2% (friccionar 30 s e deixar secar completamente). Se alergia, usar PVPI. Não repalpar após antissepsia (se necessário, usar luva estéril).
- Punção periférica com sistema fechado (butterfly) sem tocar no sítio.
- Ordem de inoculação:
- Com butterfly: aeróbio primeiro, depois anaeróbio (evita entrada de ar no anaeróbio).
- Com seringa: anaeróbio primeiro, depois aeróbio.
- Inocular o volume correto em cada frasco (adulto: 10 mL), sem ultrapassar a marca; não refrigerar.
- Homogeneizar suavemente (não agitar vigorosamente), rotular (data/hora, sítio, coletor) e enviar imediatamente ao laboratório/incubador (ideal: < 2 h).
- Registrar antes do antibiótico; se já em uso, informar horário da última dose.
d. Coleta de hemoculturas para diagnóstico de infecção relacionada a cateter vascular.
Para investigar infecção relacionada ao cateter, colho as hemoculturas ao mesmo tempo: uma por veia periférica e outra pelo próprio cateter (se tiver vários lúmens, uma de cada lúmen). Em adultos, uso o mesmo volume nos dois conjuntos (em geral 20–30 mL por conjunto, divididos em dois frascos). Antes da punção, pauso soro e antibiótico por alguns minutos e capricho na higiene: álcool 70% nas tampas dos frascos e clorexidina alcoólica 2% na pele e no hub; deixo secar bem e evito tocar de novo no local. Coletado o sangue, inoculo direto nos frascos, respeitando o volume indicado, não refrigero, identifico cada frasco com site/lúmen e horário e envio logo ao laboratório (de preferência em até 2 horas). No cateter, não descarto os primeiros mililitros, porque ajudam a mostrar colonização do lúmen. Se o cateter for retirado, envio também cerca de 5 cm da ponta para cultura, o que complementa o diagnóstico. Depois, o laboratório compara o tempo para positivar entre a amostra periférica e a do cateter; quando a do cateter dá positiva bem antes, isso reforça a suspeita de infecção ligada ao dispositivo.
ETAPA 2: Análise de erros analíticos
Você recebeu algumas reclamações da equipe médica do hospital, que diziam não estar obtendo sucesso na antibioticoterapia dos pacientes, mesmo seguindo os resultados dos antibiogramas. Na análise dos problemas demonstrados no seu controle de qualidade, você também percebeu que a leitura e interpretação dos halos de inibição do antibiograma por disco-difusão estava incompatível com os resultados esperados, indicando possíveis falhas na padronização do método. Além desse problema, os testes de controle de qualidade realizados em alguns meios de cultura diferenciais não apresentavam resultados satisfatórios em relação ao crescimento microbiológico e mudanças de cor. Depois de várias tentativas de ajustes para melhoria disso, foi decidida a troca da marca dos meios, ficando a seu critério o estudo das bulas dos produtos novos. Então, RESPONDA:
Questão 3:
O controle de variáveis físico-químicas dos ágares e do inóculo bacteriano, é fundamental para garantir a precisão, reprodutibilidade e confiabilidade dos resultados do antibiograma por disco-difusão. Sendo assim, EXPLIQUE quais são as variáveis do ágar Mueller-Hinton e da concentração do inóculo bacteriano que podem interferir no resultado do antibiograma por disco-difusão e porque isso acontece.
Nos antibiogramas por disco-difusão em ágar Mueller-Hinton, a espessura da camada (ideal ≈4 mm) influencia diretamente a difusão: meio mais espesso gera halos menores (falso resistente) e mais fino, halos maiores (falso sensível). O pH (alvo ~7,2–7,4) altera a ionização/atividade de fármacos e o crescimento, mudando diâmetros. Cátions Ca²⁺/Mg²⁺ em excesso reduzem a atividade de aminoglicosídeos e tetraciclinas (halos menores); em déficit, halos podem parecer maiores. Timidina/timina elevadas antagonizam trimetoprim/sulfametoxazol, encolhendo halos. Concentração/porosidade do gel, umidade superficial e idade/armazenamento do meio afetam crescimento e difusão (superfície molhada dilui inoculado/disco e distorce resultados). Quanto ao inóculo, a densidade deve ser 0,5 McFarland (~1–2×10⁸ UFC/mL): carga alta diminui halos (falso resistente) e carga baixa os aumenta (falso sensível). Usar colônias jovens (18–24 h), ajustar turbidez com densitômetro/padrão visual, semear lawn homogêneo e aplicar os discos/encubar em até ~15 min; atrasos, pressão/ângulo inadequados do swab e variações técnicas alteram o início do crescimento e a difusão, impactando o diâmetro final dos halos.
Questão 4:
No processo de identificação de bactérias Gram-positivas e Gram-negativas são usados meios diferenciais, como o MacConkey e o Manitol Salgado (também conhecido como Chapman). DIFERENCIE esses dois meios de cultura, abordando suas finalidades, mecanismos de ação e características colorimétricas de cada um.
MacConkey (MAC) — finalidade: seleção e diferenciação de bacilos Gram-negativos entéricos. Mecanismo de ação: sais biliares e violeta de cristal inibem Gram-positivos; lactose como carboidrato e vermelho neutro como indicador de pH diferenciam fermentadores de lactose. Colorimetria: fermentadores de lactose (p.ex., E. coli) → colônias rosa/vermelhas com possível halo de precipitado biliar; não fermentadores (p.ex., Salmonella, Shigella) → colônias incolores/translúcidas e meio amarelado-pálido.
Manitol Salgado (MSA/Chapman) — finalidade: seleção de cocos Gram-positivos halotolerantes, sobretudo estafilococos, e diferenciação de fermentadores de manitol (útil para triagem de Staphylococcus aureus). Mecanismo de ação: NaCl 7,5% inibe a maioria das bactérias não halotolerantes; manitol como carboidrato e vermelho de fenol como indicador diferenciam fermentadores. Colorimetria: fermenta manitol (p.ex., S. aureus) → meio/colônias amarelos (acidificação); não fermenta (p.ex., S. epidermidis) → meio permanece rosa/vermelho com colônias pálidas.
Questão 5:
Muitos meios são classificados como meios diferenciais, que possuem indicadores de pH ou de reações bioquímicas que mudam de cor quando o microrganismo metaboliza certos compostos. Analise as alterações dos meios de cultura de uma amostra de coprocultura e DETERMINE e JUSTIFIQUE o provável patógeno, baseando-se nas características das colônias nos meios e na coloração de Gram.
Provável patógeno: Salmonella spp. Justificativa: crescimento em MacConkey como colônias incolores (não fermenta lactose); em XLD, colônias vermelhas com centro negro e/ou em Hektoen, colônias verde-acinzentadas com centro negro (produção de H₂S); eventualmente em SS, incolores com centro negro. A Gram evidencia bacilos Gram-negativos. O conjunto “não fermentador de lactose + H₂S positivo em meios diferenciais” é característico de Salmonella enterica em coproculturas.
REFERÊNCIAS
CLINICAL AND LABORATORY STANDARDS INSTITUTE (CLSI). Performance standards for antimicrobial susceptibility testing. 35th ed. CLSI supplement M100. Wayne, PA: CLSI, 2025. Disponível em: https://clsi.org/standards/products/microbiology/documents/m100/. Acesso em: 15 ago. 2025.
EUROPEAN COMMITTEE ON ANTIMICROBIAL SUSCEPTIBILITY TESTING (EUCAST). The EUCAST disk diffusion method for antimicrobial susceptibility testing. Version 11.0. Växjö: EUCAST, 2024. Disponível em: https://www.eucast.org/ast_of_bacteria/disk_diffusion_methodology/. Acesso em: 15 ago. 2025.
UNICESUMAR. Microbiologia Clínica – Aula 1 [apresentação de slides]. Maringá: UniCesumar, 2025.
UNICESUMAR. Microbiologia Clínica – Aula 2 [apresentação de slides]. Maringá: UniCesumar, 2025.
UNICESUMAR. Microbiologia Clínica – Aula 3 [apresentação de slides]. Maringá: UniCesumar, 2025.


![1) O paciente J.S.C., 56 anos, está internado na UTI após complicações com o infarto agudo do miocárdio. Como se encontra intubado e sob ventilação mecânica, é necessário acompanhar os parâmetros ventilatórios e químicos do paciente. Para isso, amostras de sangue arterial são coletadas e analisadas no exame de gasometria. No último exame, os resultados foram pH = 7,27; pCO2 = 18 mmHg; pO2 = 81 mmHg; sO2 = 95%; [HCO3-] = 8 mM. Baseado nos resultados do último exame de gasometria do paciente J.S.C., assinale a alternativa correta. ________________________________________ Alternativas: • a) O paciente J.S.C. apresenta um quadro de alcalemia, em um processo de alcalose metabólica, pois a produção de ácido láctico durante o infarto agudo do miocárdio induziu uma produção excessiva de íon bicarbonato. • b) Devido à acidemia e à hipocapnia, a equipe interpretou o quadro do paciente como acidose respiratória. Para corrigir esse desequilíbrio ácido-base, a frequência respiratória do paciente foi reduzida para aumentar a pCO2. • c) A equipe interpretou os resultados da gasometria como um processo de alcalose respiratória, pois o paciente apresenta reduções da pCO2 e da concentração plasmática de íons bicarbonato. • d) Com o infarto agudo do miocárdio, houve um consumo do CO2 para neutralizar o excesso de ácido láctico produzido pelo miocárdio em anóxia. Por isso, a redução de pCO2 presente na gasometria. • e) Baseando-se nos resultados da gasometria, a equipe interpretou que o paciente apresentava um quadro de acidose metabólica, como pode ser visto pelas reduções da pCO2 e da [HCO3-]. 2) As proteínas são polímeros lineares construídos a partir de unidades monoméricas chamadas de aminoácidos, os quais são unidos ponta a ponta. A sequência dos aminoácidos ligados uns aos outros é chamada de estrutura primária. De maneira notável, as proteínas se dobram espontaneamente em estruturas tridimensionais, determinadas pela sequência de aminoácidos no polímero proteico. A estrutura tridimensional formada pelas pontes de hidrogênio entre os aminoácidos próximos uns dos outros é chamada de estrutura secundária, enquanto a estrutura terciária é formada por interações de longa distância entre os aminoácidos. A função da proteína depende diretamente desta estrutura tridimensional. Portanto, as proteínas são a personificação da transição de um mundo unidimensional de sequências para um mundo tridimensional de moléculas capazes de realizar diversas funções. Muitas proteínas têm estruturas quaternárias, em que a proteína funcional é composta por várias cadeias polipeptídicas. Considerando o texto da questão, analise as seguintes afirmativas: I - A estrutura primária não determina o padrão de dobramento da proteína. II - Nas estruturas terciária e quaternária, as proteínas são funcionais. III - A estrutura tridimensional independe das interações entre os aminoácidos. Considerando as informações apresentadas, é correto o que se afirma em: ________________________________________ Alternativas: • a) I, apenas. • b) II, apenas. • c) III, apenas. • d) I e III, apenas. • e) I, II e III. 3) Os monossacarídeos ou açúcares simples são as menores unidades de açúcar que não podem ser hidrolisadas em carboidratos mais simples. Os monossacarídeos, compostos de função orgânica mista, são constituídos por um esqueleto carbônico de 3 a 7 carbonos. A seguir, uma ilustração da estrutura de dois monossacarídeos. Fonte: elaborado pelo autor. Com base nas informações do texto e da figura, além dos seus conhecimentos sobre o assunto, assinale a alternativa correta. ________________________________________ Alternativas: • a) O monossacarídeo A tem 5 átomos de carbono no esqueleto carbônico e o grupo químico aldoxila. Por isso, o monossacarídeo A é classificado como pentose e aldose. • b) O monossacarídeo B possui 6 carbonos na sua estrutura carbônica e a função orgânica é aldeído. Por isso, o monossacarídeo B é classificado como hexose e aldose. • c) O monossacarídeo A e o monossacarídeo B são hexoses, porém o primeiro é uma aldose, enquanto o segundo é uma cetose. • d) O grupo químico destacado pelo círculo no monossacarídeo A é uma carboxila, por isso, esse açúcar é ácido, um tipo modificado encontrado nos glicosaminoglicanos. • e) O monossacarídeo A e o monossacarídeo B são hexoses, porém o primeiro é uma cetose, enquanto o segundo é uma aldose. 4) Após a fosforilação da glicose, em uma reação catalisada pela enzima hexocinase, a glicose-6-fosfato pode ser utilizada por várias vias metabólicas, como a glicogênese, a oxidação pela via da pentose-fosfato e oxidação pela glicólise. Esta última é a primeira etapa da oxidação completa da glicose para a produção de energia, sendo as duas outras etapas, a oxidação do piruvato e o ciclo do ácido cítrico. A glicólise tem duas fases, a preparatória e de pagamento. Em relação à glicólise, avalie as seguintes asserções e a relação proposta entre elas. I. A glicólise é um conjunto de reações químicas que ocorre apenas nas células eucarióticas e em condições exclusivamente aeróbicas. Na fase preparatória da glicólise, são formadas duas moléculas de ATP, além dos elétrons resultantes da oxidação que são transferidos para formar NADPH. Na fase de pagamento, ocorre gasto de energia para clivagem da glicose para formação de duas moléculas de piruvato. PORQUE II. As reações químicas da glicólise ocorrem no citosol, não necessitando das mitocôndrias nem de oxigênio, por isso essa via metabólica é encontrada em todos os seres vivos, de bactérias aos seres humanos. Na fase preparatória, são usadas duas moléculas de ATP para fosforilação e, portanto, há gasto de energia. Na fase de pagamento, ocorrem a formação de ATP e a transferência de elétrons para NAD+ para formação de NADH. A respeito dessas asserções, assinale a alternativa correta. ________________________________________ Alternativas: • a) As asserções I e II são proposições verdadeiras, mas II não justifica a I. • b) As asserções I e II são proposições verdadeiras e a II justifica a I. • c) A asserção I é uma proposição falsa e a II, verdadeira. • d) A asserção I é uma proposição verdadeira e a II, falsa. • e) As asserções I e II são proposições falsas. 5) Na fosforilação oxidativa, as reações de oxirredução possibilitam o fluxo de elétrons de NADH e FADH2 para o oxigênio. O fluxo de elétrons ocorre em quatro grandes complexos proteicos que estão inseridos na membrana interna da mitocôndria e juntos são denominados cadeia respiratória ou cadeia de transporte de elétrons. Três desses complexos proteicos utilizam a energia liberada pelo fluxo de elétrons para gerar um gradiente de pH e um potencial elétrico transmembrana que, por sua vez, geram a força próton-motriz. Essa força gera um fluxo de prótons, cuja energia é utilizada para formação de ATP. Portanto, a oxidação das fontes energéticas e a fosforilação do ADP para formar ATP são acopladas por um gradiente de prótons através da membrana mitocondrial interna. Considerando as informações apresentadas e os seus conhecimentos sobre o assunto, é correto o que se afirma em: ________________________________________ Alternativas: • a) NADH transfere os seus elétrons para os Complexos I, III e IV, enquanto FADH2 transfere seus elétrons para Complexo II. A partir desses complexos proteicos, os elétrons, após a ativação das bombas de prótons, são transferidos para o gás oxigênio. • b) O gás oxigênio é considerado o aceptor final de elétrons, pois neutraliza os elétrons no final da cadeia respiratória. Porém, em uma situação de anóxia, a ubiquinona e o citocromo c podem atuar como aceptores finais de elétrons para a continuidade da fosforilação oxidativa. • c) O fluxo de elétrons pela cadeia respiratória gera um gradiente eletroquímico de prótons através da membrana interna da mitocôndria que, por sua vez, gera um fluxo de prótons cuja energia é utilizada pela ATP-sintase para a formação de ATP. • d) A atividade de bombas de prótons dos Complexos I, III e IV depende da energia fornecida pelo ATP. Com isso, os elétrons são bombeados para a matriz mitocondrial, para reagirem com o gás oxigênio para a formação da água. • e) O fluxo de elétrons gera um gradiente de pH transmembrana, porém não há diferenças de concentração de prótons entre o espaço intermembranoso e a matriz mitocondrial. Por isso, a força próton-motriz é baixa para a produção de ATP.](https://normasacademicas.com/wp-content/uploads/2025/12/CAPA-25-300x214.png)